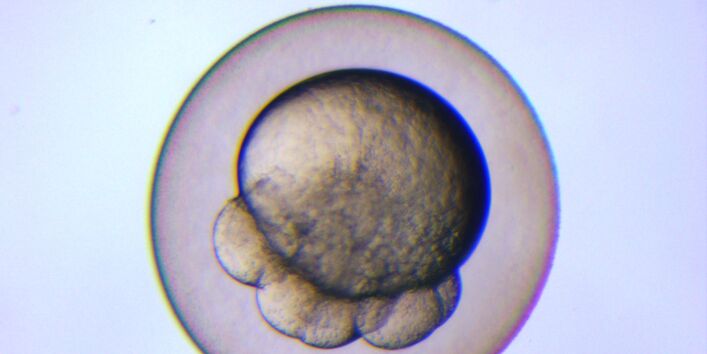
Fischembryo-Toxizitätstest
Der akute Fischtest ist als Tierversuch aus ethischen Gründen, aber auch wegen seiner hohen Kosten umstritten. Daher wurde der Fischembryo-Toxizitätstest (FET) entwickelt. Die neue Methode basiert auf dem im Abwasserbereich bereits obligatorischen Test mit Eiern des Zebrabärblings Danio rerio. Der Zebrabärbling ist ein etablierter Modellorganismus im Laborbereich. Er eignet sich besonders wegen seiner ganzjährigen, täglichen Laichbereitschaft und seines kurzen Reproduktionszyklus‘.
In diesem Biotest werden Eier des Zebrabärblings verschiedenen Konzentrationen von Stoffen oder Stoffgemischen ausgesetzt. Jeweils 24, 48, 72 und 96 Stunden nach Expositionsbeginn wird die Embryonalentwicklung auf mindestens vier charakteristische Merkmale (toxikologische/letale Endpunkte) überprüft. Diese Endpunkte sind charakteristisch für eine normale Embryonalentwicklung. Weichen sie von der unbeeinflussten Embryonalentwicklung in der Negativ-Kontrolle ab, gilt der Embryo als nicht lebensfähig. Aus dem Zusammenhang zwischen Wirkung des Stoffs/Stoffgemisches auf den Embryo und der Testkonzentration können die notwendigen Parameter für die Toxizitätsbewertung abgeleitet werden.
In Zusammenarbeit mit dem FG IV 1.1 „Internationales Chemikalienmanagement“ wurde die Aufnahme des FET in das OECD-Test Guideline Programm beantragt. Ein Ende 2005 abgeschlossenes UFOPLAN-Vorhaben (Forschungskennzeichen 203 65 422) untersuchte die Anpassung der Testmethoden im Stoffvollzug an den aktuellen Stand der Wissenschaft. Als Ergebnis wurde eine Übersicht aller derzeit vorliegenden Stoffdaten aus Fischembryonaltests erstellt und eine detaillierte Literaturstudie sowie ein ausgereifter Methodenvorschlag für den OECD-Standardisierungsprozess angefertigt.
Nach einer ausgedehnten Validierungsphase wurde der FET am 26. Juli 2013 auf der OECD-Website als „OECD Test No. 236: Fish Embryo Acute Toxicity (FET) Test“ veröffentlicht.